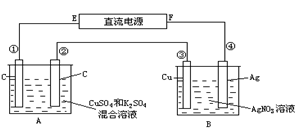
【化学---选修2:化学与技术(15分)】MgSO4·7H2O在印染、造纸和医药等工业上都有广泛的应用,利用化工厂生产硼砂的废渣-一硼镁泥可制取七水硫酸镁。硼镁泥的主要成分是MgCO3,还含有其他杂质(MgO、SiO2、Fe2O3、FeO、CaO、Al2O3、MnO等)。
表1 部分阳离子以氢氧化物形式完全沉淀时溶液的pH
沉淀物
|
Al(OH)3
|
Fe(OH)3
|
Fe(OH)2
|
Mn(OH)2
|
Mg(OH)2
|
pH值
|
5.2
|
3.2
|
9.7
|
10.4
|
11.2
|
表2 两种盐的溶解度(单位为g/100 g水)
温度/ ℃
|
10
|
30
|
40
|
50
|
60
|
CaSO4
|
0.19
|
0.21
|
0.21
|
0.20
|
0.19
|
MgSO4·7H2O
|
30.9
|
35.5
|
40.8
|
45.6
|
/
|
硼镁泥制取七水硫酸镁的工艺流程如下:
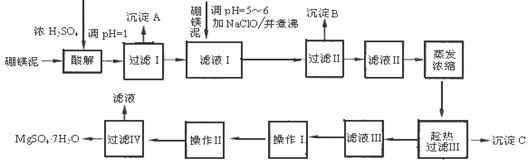
根据以上流程图并参考表格pH数据和溶解度数据,试回答下列问题:
(1)沉淀C的化学式是
(2)过滤Ⅲ需趁热过滤的理由是
(3)操作Ⅰ和操作Ⅱ的名称分别为、
(4)滤液I中加入硼镁泥,调节溶液的pH=5~6,可除去滤液Ⅰ中(填离子符号);加入NaClO溶液加热煮沸,可将Fe2+氧化成Fe3+的同时,还会将溶液中的Mn2+氧化成MnO2,写出Mn2+被氧化成MnO2的离子反应方程式为
(5)硼镁泥是硼镁矿生产硼砂(Na2B4O7·10H2O)时的废渣。将硼镁矿(Mg2B2O5·H2O)煅烧、粉碎后加水和纯碱,在加热加压下通入CO2可得硼砂。此反应为熵减小反应,试写出反应方程式