探究二:精还原铁粉是一种重要的化工原料,某兴趣小组对其进行下列研究:
【物质制备】利用绿矾制备精还原铁粉的工艺流程如下: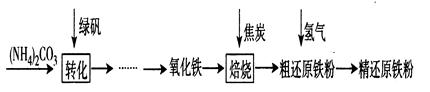
粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为FexOy + y H2 x Fe + y H2O,Fe3C + 2 H2
x Fe + y H2O,Fe3C + 2 H2 3 Fe + CH4。
3 Fe + CH4。
(1)写出焙烧中氧化铁与CO反应的化学方程式: 。
(2)焙烧中加焦炭的作用除了可以生成CO外,还能 。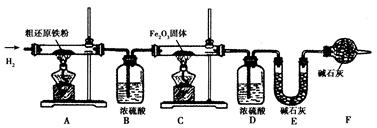
【含量测定】为得到精还原铁粉并测定粗还原铁粉中氧和碳元素的质量分数,按如下装置进行实验。已知3 CH4 + 4 Fe2O3 3 CO2 + 6H2O + 8 Fe(假设每步反应都完全,且不考虑装置内原有空气对测定结果的影响)。
3 CO2 + 6H2O + 8 Fe(假设每步反应都完全,且不考虑装置内原有空气对测定结果的影响)。
(3)主要实验步骤如下:
①按顺序组装仪器,检查装置的气密性,称量样品和必要装置的质量;②点燃A处酒精灯;③缓缓通入纯净干燥的H2;④点燃C处酒精灯;⑤分别熄灭A处、C处酒精灯;⑥再缓缓通入少量H2;⑦再次称量必要装置的质量。
操作的先后顺序是①→③→ →⑤→⑥→⑦(填字母)
A.②→④ B.④→②
(4)步骤③的目的是 ,验证该步骤目的达到的实验方法是 ;
(5)若缺少装置D,则所测氧元素的质量分数将 (填“偏大’’“偏小"或“不变")。
(6)粗还原铁粉样品的质量为20.000 g,装置B、E分别增重0.360 g和0.440 g,则计算样品出中碳元素的质量分数是 ,氧元素的质量分数是 。
 2Fe+3CO2,请写出反应器中产生一氧化碳的化学方程式:______________________.
2Fe+3CO2,请写出反应器中产生一氧化碳的化学方程式:______________________.






 粤公网安备 44130202000953号
粤公网安备 44130202000953号