根据右图装置回答: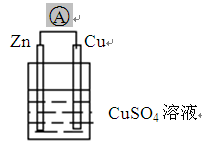
(1)原电池的负极材料是
(2)Cu片上发生 反应。(填“氧化”或“还原”)
(3)电流方向由 流向 (填“Zn”或“Cu”)
(4)写出电极反应式
负极:
正极:
总反应:
根据右图装置回答:
(1)原电池的负极材料是
(2)Cu片上发生 反应。(填“氧化”或“还原”)
(3)电流方向由 流向 (填“Zn”或“Cu”)
(4)写出电极反应式
负极:
正极:
总反应: