化合物Ⅰ是重要的化工原料,可发生下列反应生成Ⅲ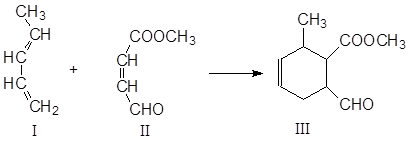
化合物Ⅰ可用石油裂解气中的2-戊烯来合成,流程如下: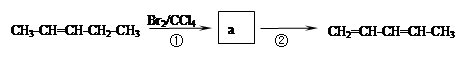
a的结构简式是______________________,②步的反应类型是_______________。
化合物I的一种同分异构体是天然橡胶的单体,用系统命名法命名该单体___________。
化合物Ⅰ与II反应还可能得到III的一种同分异构体,该物质的结构简式为__________。
欲检验化合物Ⅲ中的碳碳双键,正确的试剂是_______________________。
相关知识点
化合物Ⅰ是重要的化工原料,可发生下列反应生成Ⅲ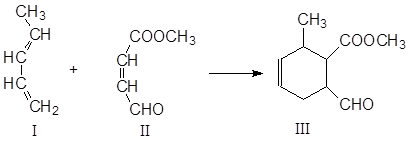
化合物Ⅰ可用石油裂解气中的2-戊烯来合成,流程如下: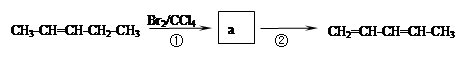
a的结构简式是______________________,②步的反应类型是_______________。
化合物I的一种同分异构体是天然橡胶的单体,用系统命名法命名该单体___________。
化合物Ⅰ与II反应还可能得到III的一种同分异构体,该物质的结构简式为__________。
欲检验化合物Ⅲ中的碳碳双键,正确的试剂是_______________________。