氢气是一种清洁、高效的新型能源。
I.用甲烷制取氢气的反应分为两步,其能量变化如下图所示:

(1)甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是。
II.在容积为1L的密闭容器内,加入0.1molCO和0.1molH2O,在催化剂存在的条件下高温加热使其反应。测得CO2的浓度随时间变化的图像如下图:
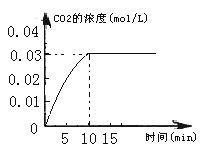
(2)在该温度下,从反应开始至达到平衡时,CO的平均反应速率为;
(3)下列改变中,能使平衡向正反应方向移动的是。
| A.升高温度 |
B.增大压强 |
| C.增大H2O(g)的浓度 |
D.减少CO2(g)的浓度 |
(4)保持温度不变,若起始时c(CO)=1mol·L—1, c(H2O)="2" mol·L—1,反应进行一段时间后,测得H2的浓度为0.4 mol·L—1。通过计算,判断此时该反应进行的方向并说明理由:。