乙烯的产量标志着一个国家的石油化工发展水平,它是很重要的工业原料.
(1)已知聚苯乙烯塑料的单体是苯乙烯(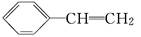 ),由苯乙烯合成聚苯乙烯塑料属于________反应;苯乙烯也能使溴水褪色,其反应的化学方程式为___________________.
),由苯乙烯合成聚苯乙烯塑料属于________反应;苯乙烯也能使溴水褪色,其反应的化学方程式为___________________.
(2)乙烯的某同系物A(化学式为C5H10)和H2加成后的产物的一氯取代物有3种,试写出A可能有的结构简式:___________________________________________________.
乙烯的产量标志着一个国家的石油化工发展水平,它是很重要的工业原料.
(1)已知聚苯乙烯塑料的单体是苯乙烯(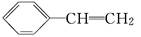 ),由苯乙烯合成聚苯乙烯塑料属于________反应;苯乙烯也能使溴水褪色,其反应的化学方程式为___________________.
),由苯乙烯合成聚苯乙烯塑料属于________反应;苯乙烯也能使溴水褪色,其反应的化学方程式为___________________.
(2)乙烯的某同系物A(化学式为C5H10)和H2加成后的产物的一氯取代物有3种,试写出A可能有的结构简式:___________________________________________________.