紫杉醇是一种新型抗癌药,其分子式为C47H51NO14,它是由如下的A酸和B醇生成的一种酯。
A. 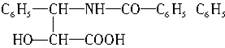 —是苯基
—是苯基
B.R—OH(R是一个含有C、H、O的基团)
(1)A可在无机酸催化下水解,其反应的方程式是___________________________。
(2)A水解所得的氨基酸,不是天然蛋白质水解产物,因为氨基不在____(填希腊字母)位。
(3)写出ROH的分子式_________________________。
紫杉醇是一种新型抗癌药,其分子式为C47H51NO14,它是由如下的A酸和B醇生成的一种酯。
A. 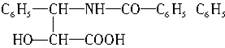 —是苯基
—是苯基
B.R—OH(R是一个含有C、H、O的基团)
(1)A可在无机酸催化下水解,其反应的方程式是___________________________。
(2)A水解所得的氨基酸,不是天然蛋白质水解产物,因为氨基不在____(填希腊字母)位。
(3)写出ROH的分子式_________________________。