某温度时0.1 mol·L-1 Na2CO3溶液中,c(Na+)/c( )=
)=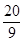 >2,其原因是(用离子方程式表示)__________________________。现向Na2CO3溶液中通入一定量的CO2后,c(Na+)/c(
>2,其原因是(用离子方程式表示)__________________________。现向Na2CO3溶液中通入一定量的CO2后,c(Na+)/c( )=
)=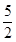 >
>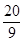 ,其原因是(用离子方程式表示)_______________________,此时c(
,其原因是(用离子方程式表示)_______________________,此时c(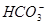 )=_________________。
)=_________________。
某温度时0.1 mol·L-1 Na2CO3溶液中,c(Na+)/c( )=
)=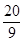 >2,其原因是(用离子方程式表示)__________________________。现向Na2CO3溶液中通入一定量的CO2后,c(Na+)/c(
>2,其原因是(用离子方程式表示)__________________________。现向Na2CO3溶液中通入一定量的CO2后,c(Na+)/c( )=
)=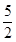 >
>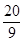 ,其原因是(用离子方程式表示)_______________________,此时c(
,其原因是(用离子方程式表示)_______________________,此时c(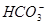 )=_________________。
)=_________________。