X、Y、Z是ⅠAⅦA族的三种非金属元素,它们在周期表中的位置如右图所示。试完成下列问题: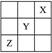
(1)X元素单质的化学式是__________。
(2)Y元素的原子结构示意图是__________,Y与Na所形成化合物的电子式为__________。
(3)Z元素的名称是__________,从元素原子得失电子的角度看,Z元素具有__________性;若从Z元素在周期表中所处位置看,它具有这种性质的原因是____________________,其价电子排布式为__________。
X、Y、Z是ⅠAⅦA族的三种非金属元素,它们在周期表中的位置如右图所示。试完成下列问题:
(1)X元素单质的化学式是__________。
(2)Y元素的原子结构示意图是__________,Y与Na所形成化合物的电子式为__________。
(3)Z元素的名称是__________,从元素原子得失电子的角度看,Z元素具有__________性;若从Z元素在周期表中所处位置看,它具有这种性质的原因是____________________,其价电子排布式为__________。