已知氯水中有如下平衡: 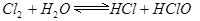 。常温下,在一个体积为50mL的针筒里吸入40mL氯气后,再吸进10mL水。写出针筒中可能观察到的现象_______________ ______。可将此针筒
。常温下,在一个体积为50mL的针筒里吸入40mL氯气后,再吸进10mL水。写出针筒中可能观察到的现象_______________ ______。可将此针筒
长时间放置,又可能看到何种变化___ ____;试用平衡观点加以解释 。
已知氯水中有如下平衡: 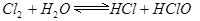 。常温下,在一个体积为50mL的针筒里吸入40mL氯气后,再吸进10mL水。写出针筒中可能观察到的现象_______________ ______。可将此针筒
。常温下,在一个体积为50mL的针筒里吸入40mL氯气后,再吸进10mL水。写出针筒中可能观察到的现象_______________ ______。可将此针筒
长时间放置,又可能看到何种变化___ ____;试用平衡观点加以解释 。