A、B、C、D分别是NaNO3、NaOH、HNO3和Ba(NO3)24种溶液中的一种,现利用另一种溶液X,用如图所示方法可将它们依次确定。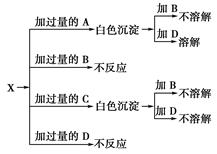
试确定A、B、C、D、X各代表哪种溶液。
A________,B________,C________,D________,X________。
A、B、C、D分别是NaNO3、NaOH、HNO3和Ba(NO3)24种溶液中的一种,现利用另一种溶液X,用如图所示方法可将它们依次确定。
试确定A、B、C、D、X各代表哪种溶液。
A________,B________,C________,D________,X________。