根据下列实验装置图填空: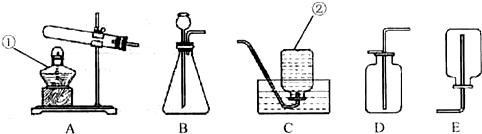
(1)写出上图所示装置中标有序号的仪器名称:① ② 。
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,应选择的发生装置是 , 收集装置是 ,反应的方程式是 。
(3)氨气是一种无色有刺激性气味、极易溶于水、密度比空气小的气体.实验室常用加热氯化铵和熟石灰的固体混合物制取氨气,则其发生装置应选择 ,收集装置应选择 。
根据下列实验装置图填空:
(1)写出上图所示装置中标有序号的仪器名称:① ② 。
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,应选择的发生装置是 , 收集装置是 ,反应的方程式是 。
(3)氨气是一种无色有刺激性气味、极易溶于水、密度比空气小的气体.实验室常用加热氯化铵和熟石灰的固体混合物制取氨气,则其发生装置应选择 ,收集装置应选择 。