某学校化学学习小组同学设计出下图所示装置,并进行白磷燃烧实验。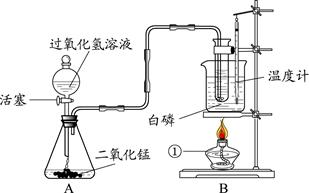
(1)图中标“①”的仪器名称是 。
(2)图A可用于实验室制氧气,其反应的化学方程式为 ,氧气的收集方法是 或 。
(3)当烧杯内的水受热,温度计显示30℃时,打开图A中分液漏斗的玻璃塞和活塞,在图B中盛有水的试管中有气泡均匀逸出,白磷未燃烧,白磷未燃烧的原因是 。
(4)随着水温升高,温度计显示40℃时,再次打开活塞,白磷在水里燃烧。白磷燃烧的化学方程式为 。
某学校化学学习小组同学设计出下图所示装置,并进行白磷燃烧实验。
(1)图中标“①”的仪器名称是 。
(2)图A可用于实验室制氧气,其反应的化学方程式为 ,氧气的收集方法是 或 。
(3)当烧杯内的水受热,温度计显示30℃时,打开图A中分液漏斗的玻璃塞和活塞,在图B中盛有水的试管中有气泡均匀逸出,白磷未燃烧,白磷未燃烧的原因是 。
(4)随着水温升高,温度计显示40℃时,再次打开活塞,白磷在水里燃烧。白磷燃烧的化学方程式为 。