小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质质量分数为10%。老师说,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或是碳酸钠中的一种。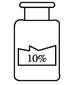
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,认为该溶液不可能是氢氧化钙溶液,理由是 。
(2)小亮取少量样品于试管中,滴加 试液,试液变红色,该溶液不可能是 。
(3)为了进一步确定该溶液的成分,小亮设计了以下实验方案:
方案A:选择稀盐酸来确定该溶液的成分;
方案B:选择无色酚酞试液来确定该溶液的成分;
你认为以上方案中合理的是 ,若选择一种常见的碱溶液来确定,有关反应
的化学方程式为 。
(4)小亮通过上述方法证明该溶液的成分为NaOH,于是他取一定体积的NaOH溶液
(20℃),并向其中滴加10%的盐酸(20℃),测得反应中溶液的温度与加入盐酸体积的变化如下。
| 加入盐酸的体积(V)/mL |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
16 |
18 |
20 |
| 溶液温度 (t)/℃ |
25.2 |
29.6 |
32.0 |
36.0 |
38.2 |
36.7 |
35.7 |
34.7 |
33.7 |
32.9 |
根据上表分析溶液温度变化的原因:
①加入盐酸的量在2~10 mL之间时 。
②加入盐酸的量在10~20 mL之间时 。
 法。实验过程是:
法。实验过程是: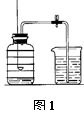
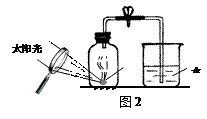

 _。
_。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号