煤燃烧排放的烟含有
和
, 形成酸雨、污染大气,采用
溶液作为吸收剂可同时对烟气进行脱硫、脱硝.回答下列问题:
(1)
的化学名称为________.
(2)在鼓泡反应器中通入含
、
的烟气,反应温度323K,
溶液浓度为
. 反应一段时间后溶液中离子浓度的分析结果如表.
|
离子 |
|
|
|
|
|
|
c/
|
|
|
|
|
|
①写出
溶液脱硝过程中主要反应的离子方程式________.增加压强,NO的转化率________(填"提高"、"不变"或"降低").
②随着吸收反应的进行,吸收剂溶液的pH逐渐________(填"增大"、"不变"或"减小").
③由实验结果可知,脱硫反应速率________脱硝反应速率(填"大于"或"小于")原因是除了
和NO在烟气中初始浓度不同,还可能是________.
(3)在不同温度下,
溶液脱硫、脱硝的反应中
和NO的平衡分压
如图所示.
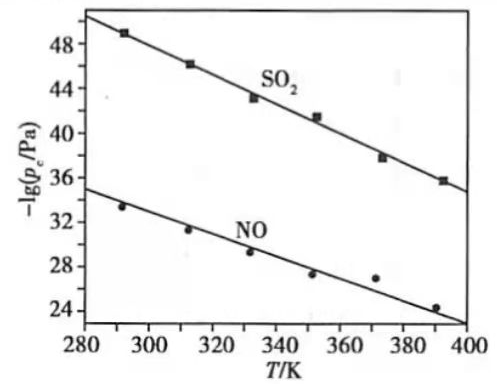
①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均______(填"增大"、"不变"或"减小").
②反应
的平衡常数K表达式为________.
(4)如果采用
、
替代
,也能得到较好的烟气脱硫效果.
①从化学平衡原理分析,
相比
具有的优点是________.
②已知下列反应:
则反应
(aq)的△H=________.
 HCl+HClO。为了探究HClO的漂白性,某同学设计了如下的实验。
HCl+HClO。为了探究HClO的漂白性,某同学设计了如下的实验。
 HCl+HClO。为了探究HClO的漂白性,某同学设计了如下的实验。
HCl+HClO。为了探究HClO的漂白性,某同学设计了如下的实验。