(23分)工业上一般在恒容密闭容器中用H2和CO生产燃料甲醇,反应方程式为CO(g)+2H2(g)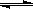 CH3OH(g)△H
CH3OH(g)△H
(1)下表所列数据是反应在不同温度下的化学平衡常数(K)。
| 温度 |
250°C |
300°C |
350°C |
| K |
2.041 |
0.270 |
0.012 |
①由表中数据判断△H 0(填“>”、“=”或“<“)
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为 ,此时的温度为 。
(2)在100℃压强为0.1 MPa条件下,容积为V L某密闭容器中a mol CO与 2a mol H2在催化剂作用下反应生成甲醇,达平衡时CO的转化率为50%,则100℃该反应的的平衡常数K= (用含a、V的代数式表示并化简至最简单的形式)。此时保持温度容积不变,再向容器中充入a mol CH3OH(g),平衡 (向正反应方向、向逆反应方向)移动,再次达到新平衡时,CO的体积分数 。(减小、增大、不变)
(3)要提高CO的转化率,可以采取的措施是 。
A.升温 B.加入催化剂 C.增加CO的浓度 D.恒容充入H2
E.恒压充入惰性气体 F.分离出甲醇
(4)判断反应达到平衡状态的依据是(填字母序号,下同) 。
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的相对平均分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
(5)300°C,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡的有关数据如下:
| 容器 |
甲 |
乙 |
丙 |
|
| 反应物投入量 |
1molCO、2moL H2 |
1molCH3OH |
2molCH3OH |
|
| 平衡 时的 数据 |
CH3OH浓度(mol/L) |
c1 |
c2 |
c3 |
| 反应的能量变化 |
akJ |
bkJ |
ckJ |
|
| 体系压强(Pa) |
p1 |
p2 |
p3 |
|
| 反应物转化率 |
α1 |
α2 |
α3 |
请选择正确的序号填空(不定项选择)
①c1、c2、c3的关系表达正确的为
A.c3>2c1 B.c1<c3<2c1 C.c1=c2
②a、b、c的关系表达正确的为
A.c<2|△H| B.a+b=|△H| C.c=2b
③p1、p2、p3的关系不正确的为
A.p1=p2 B.p2<p3<2p2 C.p3>2p2
④α1、α2、α3的关系表达不正确的为
A.α1=α2 B.α3<α2 C.α1+α2="1"
 ,
, 法。
法。 及一些硫酸盐。要将粗盐提纯,可先将粗盐溶解,按一定的顺序加入沉淀剂,再;然后将溶液调成中性并就可以得到较为纯净的氯化钠。
及一些硫酸盐。要将粗盐提纯,可先将粗盐溶解,按一定的顺序加入沉淀剂,再;然后将溶液调成中性并就可以得到较为纯净的氯化钠。 分)以石灰石、水、纯碱为原料,如何制取烧碱?写出有关反应的化学方程式,并说明基本反应类型。
分)以石灰石、水、纯碱为原料,如何制取烧碱?写出有关反应的化学方程式,并说明基本反应类型。 粤公网安备 44130202000953号
粤公网安备 44130202000953号