(6分)室温下,单质A.B、C分别为金属单质、黄绿色气体、无色气体,在一定的条件下,它们可以按下列框图进行反应。又知D溶液是黄色的。请回答: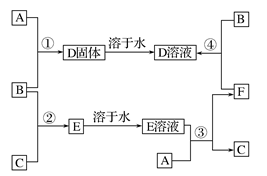
(1)写出下列物质的化学式:A________________,B____________。
(2)反应①的化学方程式:________________________________。
(3)反应④的离子方程式:________________________________。
(6分)室温下,单质A.B、C分别为金属单质、黄绿色气体、无色气体,在一定的条件下,它们可以按下列框图进行反应。又知D溶液是黄色的。请回答:
(1)写出下列物质的化学式:A________________,B____________。
(2)反应①的化学方程式:________________________________。
(3)反应④的离子方程式:________________________________。