化学科学在药物的开发、合成和使用中起着至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可治疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式: 。
(2)自选合适的氧化剂,将补铁剂中的Fe2+氧化成Fe3+,写出相关的离子反应方程式:_________________ ___。
(3)检验Fe3+常用的试剂除碱外,还可以用 (填化学式),现象是 。
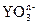 和S2-发生反应的离子方程式如下:
和S2-发生反应的离子方程式如下: Y-+3S↓+3H2O
Y-+3S↓+3H2O 粤公网安备 44130202000953号
粤公网安备 44130202000953号