原子序数依次递增的A、B、C、D、E是周期表中前30号元素。已知A的最外层电子数是其内层电子数的2倍;A与C形成的常见化合物之一是主要的温室气体;D与A同主族,其单质在同周期元素所形成的单质中熔点最高;E原子M能层为全充满状态,且核外的未成对电子只有一个。请回答下列问题:
(1)B在周期表中的位置是: ,该主族元素的气态氢化物中,沸点最低的是 (填化学式)。
(2)根据等电子原理分析,BC2+ 中B原子的轨道杂化类型是 。
(3)五种元素中,电负性最大与最小的两种非金属元素形成的化合物在常温下是晶体,其晶体类型是 。
(4)+1价气态基态阳离子再失去一个电子形成+2价气态基态阳离子所需要的能量称为第二电离能I2,依次还有I3、I4、I5…,推测D元素的电离能突增应出现在第 电离能。
(5)A的一种相对分子质量为28的氢化物,其分子中σ键与π键的个数之比为 ;;
(6)E的基态原子有 种形状不同的原子轨道;E2+ 的价电子排布式为 ;下
图(填甲、乙或丙) 表示的是E晶体中微粒的堆积方式。


甲 乙 丙
 2%和7.32%。
2%和7.32%。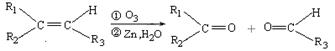 (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)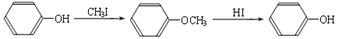
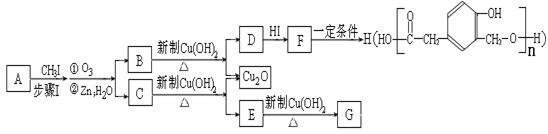
 ;
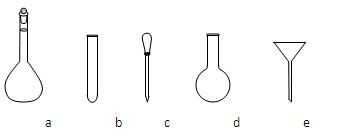
;
 H-的浓度
H-的浓度 Ca2++2A-
Ca2++2A-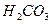


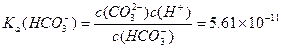

 粤公网安备 44130202000953号
粤公网安备 44130202000953号