(12分)在一定条件下,二氧化硫和氧气发生如下反应:
2SO2(g)+O2(g)  2SO3(g) ΔH<0
2SO3(g) ΔH<0
(1) 写出该反应的化学平衡常数表达式K=______ ____。降低温度,该反应K值___ ___,二氧化硫转化率______,化学反应速率___ ___。(以上均填“增大”“减小”或“不变”)
(2) 600 ℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图所示,反应处于平衡状态的时间是____ ____。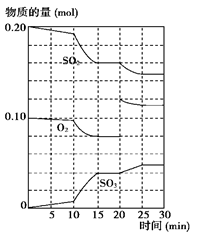
(3)据上图判断,反应进行至20 min时,曲线发生变化的原因是________________ ___________________ (用文字表达);10 min到15 min的曲线变化的原因可能是________(填写编号)。
a.加了催化剂 b.缩小容器体积
c.降低温度 d.增加SO3的物质的量
(4)已知在600℃时,2SO2(g)+O2(g)  2SO3(g)的平衡常数K=19,若600℃时测得容器内c(SO2)=0.3mol/L,c(O2)=0.1mol/L,c(SO3)=0.4mol/L,在这种情况下,该反应是否处于平衡状态? (填“是”或“否”)。此时,化学反应速率是v(正) v(逆)(填“>”、“<”或“=”),原因是 。
2SO3(g)的平衡常数K=19,若600℃时测得容器内c(SO2)=0.3mol/L,c(O2)=0.1mol/L,c(SO3)=0.4mol/L,在这种情况下,该反应是否处于平衡状态? (填“是”或“否”)。此时,化学反应速率是v(正) v(逆)(填“>”、“<”或“=”),原因是 。
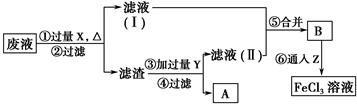
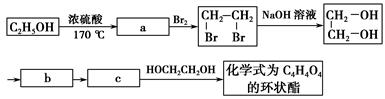
 ,十二烷基苯磺酸钠是普通洗衣粉的主要成分。其结构可用图形
,十二烷基苯磺酸钠是普通洗衣粉的主要成分。其结构可用图形 来表示,•端为链烃基,O端为极性基。根据这一结构特点,试分析和回答下列问题:
来表示,•端为链烃基,O端为极性基。根据这一结构特点,试分析和回答下列问题:



 粤公网安备 44130202000953号
粤公网安备 44130202000953号