已知空气的主要成分是氮气和氧气,某课外活动小组设计测定空气中氧气含量的实验,实验装置如图所示: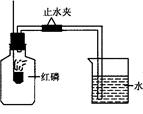
⑴该实验中红磷须稍过量,目的是 。
⑵待燃烧停止,白烟消失并冷却后,打开止水夹,观察到烧杯中的水进入集气瓶,瓶内水量约是集气瓶体积的 ,由本实验还可以推知氮气的哪一性质?试写出其中一种 。
⑶若将红磷换成炭粉,该实验能否获得成功? ,理由是 。
已知空气的主要成分是氮气和氧气,某课外活动小组设计测定空气中氧气含量的实验,实验装置如图所示:
⑴该实验中红磷须稍过量,目的是 。
⑵待燃烧停止,白烟消失并冷却后,打开止水夹,观察到烧杯中的水进入集气瓶,瓶内水量约是集气瓶体积的 ,由本实验还可以推知氮气的哪一性质?试写出其中一种 。
⑶若将红磷换成炭粉,该实验能否获得成功? ,理由是 。