下图是一种用于显示事物异同点的信息处理方法。图1中两个圆分别代表碳酸钠和碳酸氢钠的有关信息,两圆重叠区域表示它们的共同特点(相似点),重叠区域以外的部分表示它们独有的特征(不同点)。请你在图下的空格内填写适当内容。(每处只要求填一点)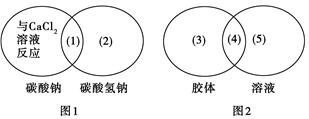
(1)________;(2)________;(3)________;(4)________;(5)________。
下图是一种用于显示事物异同点的信息处理方法。图1中两个圆分别代表碳酸钠和碳酸氢钠的有关信息,两圆重叠区域表示它们的共同特点(相似点),重叠区域以外的部分表示它们独有的特征(不同点)。请你在图下的空格内填写适当内容。(每处只要求填一点)
(1)________;(2)________;(3)________;(4)________;(5)________。