T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质的量变化如图1所示,3分钟时达到平衡;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示。 
(1)容器中发生的反应可表示为______ ________ ________ __
(2)该反应的△H 0(填“>”、“<”或“=”)
判断理由是:______ ________ ________ ________ ____ ________ __。
(3)反应进行的前3 min内,用X表示的反应速率 v(X)=____________
(4)保持其他条件不变,升高温度,该反应的化学平衡常数K将____________(填“变大”、“减小”或“不变”)
(5)①若改变反应条件,使反应进程如图3所示,则改变的条件是____________
②一定条件下的密闭容器中,该反应达到平衡,要提高气体Y的转化率,可以采取的措施是__________(填字母代号)。
a.高温高压 b.加入催化剂 c.增加X的浓度 d.增加气体Y的浓度

 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
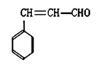 和化合物Ⅱ
和化合物Ⅱ 在一定条件下发生反应能生成化合物III
在一定条件下发生反应能生成化合物III ,请回答以下问题。
,请回答以下问题。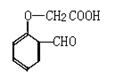 在一定条件下能发生类似化合物I和化合物II生成化合物III的反应,请写出类似化合物III的生成物的结构简式 。
在一定条件下能发生类似化合物I和化合物II生成化合物III的反应,请写出类似化合物III的生成物的结构简式 。 2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示。
2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示。
 族
族 粤公网安备 44130202000953号
粤公网安备 44130202000953号