A—E五种元素中,除A、B外其他均为短周期元素它们的性质或原子结构如下表:
| 元素 |
元素性质或原子结构 |
| A |
单质为生活中常见的金属,该金属的两种黑色氧化物(其中一种有磁性)的相对分子质量相差160 |
| B |
单质为生活中常见的金属,其相对原子质量比A大8 |
| C |
地壳中含量最多的金属元素 |
| D |
元素的主族序数是其所在周期序数的3倍 |
| E |
E的某种原子的原子核内没有中子 |
(1)C单质在强碱溶液反应的离子方程式是
(2)①在高温条件下,将D、E组成的气态化合物与A的粉末充分反应,生成8gE的单质和相应的固态化合物时,放出a KJ热量,此反应的热化学方程式是
②A的某种氯化物溶液呈黄色,向其中通入足量SO2气体,溶液变为浅绿色,此反应的离子方程式是
(3)向2mL 0.5mol/L的ACl3溶液中加入3mL 3mol/L KF溶液,ACl3溶液褪成无色,再加入KI溶液和CCl4振荡后静置,CCl4层不显色,则下列说法正确的是(已知氧化性Fe3+>I2)
(填字母)。
a. A3+不与I-发生反应 b. A3+与F-结合生成不与I-反应的物质
c. F-使I-的氧化性减弱 d. A3+被F-还原为A2+,使溶液中不再存在A3+


 达到平衡:
达到平衡: 、y、z间的关系是________________;
、y、z间的关系是________________; ,在增大压强时,若平衡发生移动,则一定向________(填“正”或“逆”)反应方向移动;
,在增大压强时,若平衡发生移动,则一定向________(填“正”或“逆”)反应方向移动; 电离度
电离度 的数值,其实验方案可设计如下:
的数值,其实验方案可设计如下: __________。
__________。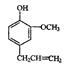 )是一种重要的调味剂,它与F的关系是。
)是一种重要的调味剂,它与F的关系是。
 CH3OH(g)某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见下图:
CH3OH(g)某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见下图:


 粤公网安备 44130202000953号
粤公网安备 44130202000953号