下列说法正确的是:( )
A.反应A(g) 2B(g);△H,若正反应的活化能为Ea kJ mol-1,逆反应的活化能为Eb kJ·mol-1,则△H=(Ea-Eb)kJ·mol-1 2B(g);△H,若正反应的活化能为Ea kJ mol-1,逆反应的活化能为Eb kJ·mol-1,则△H=(Ea-Eb)kJ·mol-1 |
| B.已知25℃时,有关弱酸的电离平衡常数:HCN Ka=4.9×10-10; H2CO3 Ka1=4.3×10-7,Ka2=5.6×10-11。则CO2通入NaCN溶液中反应的化学方程式为:2NaCN+H2O+CO2=2HCN+Na2CO3 |
C.已知: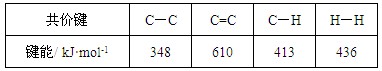 则反应 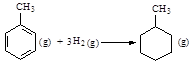 的焓变为ΔH = -384 kJ·mol-1 的焓变为ΔH = -384 kJ·mol-1 |
| D.一定浓度的NaOH溶液,温度升高PH值不变 |

 n[NaOH]=1:2
n[NaOH]=1:2 H2O+ CO32- = 2HCO3-
H2O+ CO32- = 2HCO3- 粤公网安备 44130202000953号
粤公网安备 44130202000953号