现有分子式为C9H8O2X2(X为一未知元素)的有机化合物M,可在一定条件下发生如下图所示反应: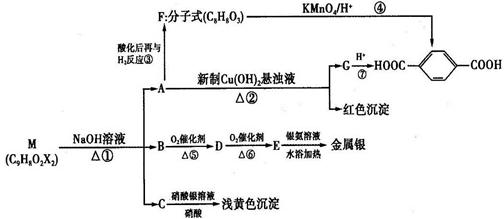
试回答下列问题:
⑴写出下列物质的结构简式:M 、F 。
⑵写出B与E反应的化学方程式:
,该反应的反应类型为 。
⑶写出与F互为同分异构体,且同时符合下列四个条件的结构简式:
①属于酯;②属于酚;③不能发生银镜反应;④苯环上的一氯取代物只有两种。
现有分子式为C9H8O2X2(X为一未知元素)的有机化合物M,可在一定条件下发生如下图所示反应:
试回答下列问题:
⑴写出下列物质的结构简式:M 、F 。
⑵写出B与E反应的化学方程式:
,该反应的反应类型为 。
⑶写出与F互为同分异构体,且同时符合下列四个条件的结构简式:
①属于酯;②属于酚;③不能发生银镜反应;④苯环上的一氯取代物只有两种。