(8分)(1)有下图所示A、B、C、D、E、 F六种仪器: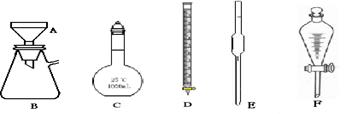
请按要求写出部分仪器的名称,填入相应的空格内:
有标准线但无0刻度的 ,通常是陶瓷质地的 。若用A、B进行抽滤,其目的主要是 。
(2)设计实验方案鉴别碳酸钠、氯化钠、硫酸钠、亚硝酸钠四种固体。请画出必要的实验流程图(写清楚主要步骤、试剂、现象、结论)。
(8分)(1)有下图所示A、B、C、D、E、 F六种仪器:
请按要求写出部分仪器的名称,填入相应的空格内:
有标准线但无0刻度的 ,通常是陶瓷质地的 。若用A、B进行抽滤,其目的主要是 。
(2)设计实验方案鉴别碳酸钠、氯化钠、硫酸钠、亚硝酸钠四种固体。请画出必要的实验流程图(写清楚主要步骤、试剂、现象、结论)。