将3 mol A和2.5 mol B混合于2L的密闭容器中,发生反应的化学方程式为:3A(气) + B(气) 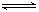 xC(气) + 2D(气),5 min后反应达到平衡状态,容器内的压强变小,已知D的平均反应速度为 0.1 mol/(L﹒min), 填写下列空白:
xC(气) + 2D(气),5 min后反应达到平衡状态,容器内的压强变小,已知D的平均反应速度为 0.1 mol/(L﹒min), 填写下列空白:
(1) x =______
(2) 平衡时C的浓度为 ________________
(3) 平衡时B的转化率为 _____________
(4) 平衡时,容器内的压强与原容器内压强的比值为 ___________
将3 mol A和2.5 mol B混合于2L的密闭容器中,发生反应的化学方程式为:3A(气) + B(气) 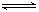 xC(气) + 2D(气),5 min后反应达到平衡状态,容器内的压强变小,已知D的平均反应速度为 0.1 mol/(L﹒min), 填写下列空白:
xC(气) + 2D(气),5 min后反应达到平衡状态,容器内的压强变小,已知D的平均反应速度为 0.1 mol/(L﹒min), 填写下列空白:
(1) x =______
(2) 平衡时C的浓度为 ________________
(3) 平衡时B的转化率为 _____________
(4) 平衡时,容器内的压强与原容器内压强的比值为 ___________