氢氧化钠是一种重要的化工基础原料,广泛地应用于造纸、纺织、石油化工、印染等行业。
(1)氢氧化钠的俗名是(只写一种)。氢氧化钠与硫酸反应的化学方程式为
。
(2)实验室有一瓶久置的固体,标签上写着"氢氧化钠"。为了检验里面是否还存在
,实验员取少量该固体样品进行以下实验:
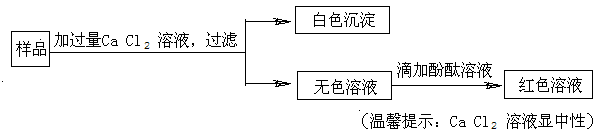
根据溶液变红这一现象说明样品中含有(填序号)。
| A. | B. | C. | D. | 和 |
如果白色沉淀中含有两种物质,这两种物质是(填化学式)。
氢氧化钠是一种重要的化工基础原料,广泛地应用于造纸、纺织、石油化工、印染等行业。
(1)氢氧化钠的俗名是(只写一种)。氢氧化钠与硫酸反应的化学方程式为
。
(2)实验室有一瓶久置的固体,标签上写着"氢氧化钠"。为了检验里面是否还存在
,实验员取少量该固体样品进行以下实验:

根据溶液变红这一现象说明样品中含有(填序号)。
| A. | B. | C. | D. | 和 |
如果白色沉淀中含有两种物质,这两种物质是(填化学式)。