下图为原电池的示意图。请回答: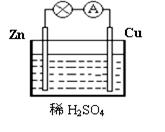
(1)Zn极为原电池的 (填“正”或“负”)极,该极的电极反应式是 ,属于 (填“氧化反应”或“还原反应”)。
(2) (填“电子”或“电流”)从锌片通过导线流向铜片,溶液中的H+从 (填“锌片”或“铜片”)获得电子
下图为原电池的示意图。请回答:
(1)Zn极为原电池的 (填“正”或“负”)极,该极的电极反应式是 ,属于 (填“氧化反应”或“还原反应”)。
(2) (填“电子”或“电流”)从锌片通过导线流向铜片,溶液中的H+从 (填“锌片”或“铜片”)获得电子