可逆反应:mA(g)+nB(g)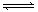 pC(g)+qD(g),根据图回答:
pC(g)+qD(g),根据图回答: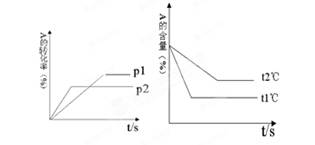
(1)压强P1比P2 (填大或小); (2)(m +m)比(p +q) (填大或小);
(3)温度t1℃比t2℃ (填高或低);(4)正反应为 反应(填吸热或放热);
(5)一定温度下,该可逆反应的平衡常数表达式为:K=
可逆反应:mA(g)+nB(g)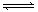 pC(g)+qD(g),根据图回答:
pC(g)+qD(g),根据图回答:
(1)压强P1比P2 (填大或小); (2)(m +m)比(p +q) (填大或小);
(3)温度t1℃比t2℃ (填高或低);(4)正反应为 反应(填吸热或放热);
(5)一定温度下,该可逆反应的平衡常数表达式为:K=