金属晶体是面心立方体,立方体的每个面5个金原子紧密堆砌(如图其余各面省略),金原子半径为d m,求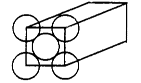
(1)金晶体中最小的一个立方体含有__________个金属原子。
(2) 欲计算一个晶胞的体积,除假定金原子是刚性小球外,还应假定 ;
(3)计算一个晶胞的体积是 cm3;
(4)金的密度为_________g•cm-3。
(5)列式计算金原子的空间利用率
金属晶体是面心立方体,立方体的每个面5个金原子紧密堆砌(如图其余各面省略),金原子半径为d m,求
(1)金晶体中最小的一个立方体含有__________个金属原子。
(2) 欲计算一个晶胞的体积,除假定金原子是刚性小球外,还应假定 ;
(3)计算一个晶胞的体积是 cm3;
(4)金的密度为_________g•cm-3。
(5)列式计算金原子的空间利用率