某小组利用下列实验数据,计算金属M的相对原子质量。已知金属M和硫酸反应的化学方程式为: M + H2SO4 ="=" MSO4 + H2↑。现取20 g该金属样品于烧杯中,然后向其中加入稀硫酸,实验数据记录如下: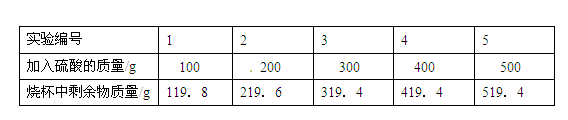
第5次实验后,烧杯中还有0.5 g剩余固体。
(1)原金属样品中M的质量
(2)计算该金属的相对原子质量。
某小组利用下列实验数据,计算金属M的相对原子质量。已知金属M和硫酸反应的化学方程式为: M + H2SO4 ="=" MSO4 + H2↑。现取20 g该金属样品于烧杯中,然后向其中加入稀硫酸,实验数据记录如下:
第5次实验后,烧杯中还有0.5 g剩余固体。
(1)原金属样品中M的质量
(2)计算该金属的相对原子质量。