如图所示,甲容器容积不变,乙容器有可移动活塞。甲中充入3mol A和2 mol B,乙中充入2 mol C和2 mol D,发生反应:3A (g) + 2B(s)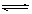 C(g) +D(g);△H>0。在相同温度下反应达到平衡,活塞移动到4处。下列有关说法正确的是( )
C(g) +D(g);△H>0。在相同温度下反应达到平衡,活塞移动到4处。下列有关说法正确的是( )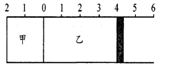
A.平衡后,容器内压强:p甲 >p乙
B.平衡后,若向乙中再加入B物质,活塞向右移动
C.同时升高相同温度,达到新平衡时,甲中A物质的速率等于乙中A物质的速率
D.平衡后,若将活塞移动至6处,乙中c(A),c(D)均减小
如图所示,甲容器容积不变,乙容器有可移动活塞。甲中充入3mol A和2 mol B,乙中充入2 mol C和2 mol D,发生反应:3A (g) + 2B(s)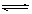 C(g) +D(g);△H>0。在相同温度下反应达到平衡,活塞移动到4处。下列有关说法正确的是( )
C(g) +D(g);△H>0。在相同温度下反应达到平衡,活塞移动到4处。下列有关说法正确的是( )
A.平衡后,容器内压强:p甲 >p乙
B.平衡后,若向乙中再加入B物质,活塞向右移动
C.同时升高相同温度,达到新平衡时,甲中A物质的速率等于乙中A物质的速率
D.平衡后,若将活塞移动至6处,乙中c(A),c(D)均减小