如图所示装置为在直流电的作用下电解CuSO4溶液图,其中A、B为石墨电极,a、b为电源的两极,当接通电源后,通电一段时间后,将B电极取出洗干净并干燥后称量其质量增加了3.2g,则: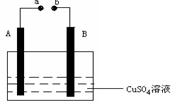
⑴a为电源的 极。
⑵写出电极反应方程式:A ,B 。
⑶如果想使反应溶液恢复到原来状态,应该加入 ,加入 g。
如图所示装置为在直流电的作用下电解CuSO4溶液图,其中A、B为石墨电极,a、b为电源的两极,当接通电源后,通电一段时间后,将B电极取出洗干净并干燥后称量其质量增加了3.2g,则:
⑴a为电源的 极。
⑵写出电极反应方程式:A ,B 。
⑶如果想使反应溶液恢复到原来状态,应该加入 ,加入 g。