某同学应用如下所示装置研究物质的性质。其中气体m的主要成分是氯气,还含有少量空气和水蒸气。请回答下列问题: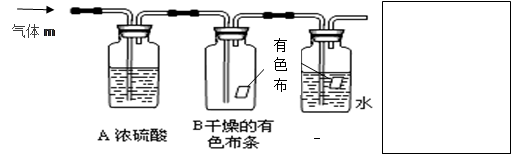
(1)浓硫酸的作用是_______________。
(2)B中观察到的实验现象是 。
(3)从物质性质方面来看,这样的实验设计还存在事故隐患,应如何处理,请用离子方程式表达原理并画出装置图(填在上图内),
某同学应用如下所示装置研究物质的性质。其中气体m的主要成分是氯气,还含有少量空气和水蒸气。请回答下列问题:
(1)浓硫酸的作用是_______________。
(2)B中观察到的实验现象是 。
(3)从物质性质方面来看,这样的实验设计还存在事故隐患,应如何处理,请用离子方程式表达原理并画出装置图(填在上图内),