利用氧化还原反应原理配平
⑴ NH3 + Cl2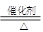 N2 + NH4Cl
N2 + NH4Cl
⑵ FeSO4 + KNO3 + H2SO4 = K2SO4 + Fe2(SO4)3 + NO↑+ H2O
在(2)的反应中 元素被氧化, 是还原产物,该反应中体现硫酸的 性。当反应中有0.3mol电子发生转移时,生成NO的体积(标准状况) L。
利用氧化还原反应原理配平
⑴ NH3 + Cl2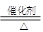 N2 + NH4Cl
N2 + NH4Cl
⑵ FeSO4 + KNO3 + H2SO4 = K2SO4 + Fe2(SO4)3 + NO↑+ H2O
在(2)的反应中 元素被氧化, 是还原产物,该反应中体现硫酸的 性。当反应中有0.3mol电子发生转移时,生成NO的体积(标准状况) L。