恒温下,将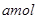
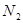 与
与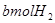 的混合气体通入一个固定容积的密闭容器中,发生如下反应:
的混合气体通入一个固定容积的密闭容器中,发生如下反应: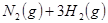

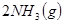
(1)若反应进行到某时刻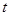 时,
时,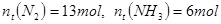 ,则a=_______。
,则a=_______。
(2)反应达平衡时,混合气体的体积为716.8L(标准状况下),其中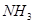 的含量(体积分数)为25%,平衡时
的含量(体积分数)为25%,平衡时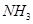 的物质的量__________。
的物质的量__________。
(3)原混合气体中,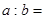 __________。
__________。
(4)达到平衡时,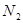 和
和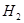 的转化率之比,
的转化率之比,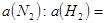 __________。
__________。
恒温下,将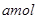
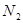 与
与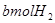 的混合气体通入一个固定容积的密闭容器中,发生如下反应:
的混合气体通入一个固定容积的密闭容器中,发生如下反应: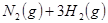

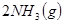
(1)若反应进行到某时刻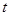 时,
时,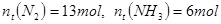 ,则a=_______。
,则a=_______。
(2)反应达平衡时,混合气体的体积为716.8L(标准状况下),其中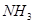 的含量(体积分数)为25%,平衡时
的含量(体积分数)为25%,平衡时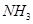 的物质的量__________。
的物质的量__________。
(3)原混合气体中,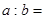 __________。
__________。
(4)达到平衡时,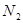 和
和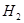 的转化率之比,
的转化率之比,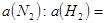 __________。
__________。