(10海南45)气焊和气割都需要用到乙炔。乙炔俗称电石气(化学式为C2H2),是一种无色无味的气体,密度比空气略小,难溶于水。实验室常用块状固体碳化钙与水反应制备乙炔,该反应比二氧化锰催化过氧化氢分解更加剧烈。请回答:
(1)乙炔的物理性质之一是 ;
(2)图中仪器a的名称是 ;
(3)从下图选择实验室制备乙炔所用仪器的最佳组合是 (填序号)。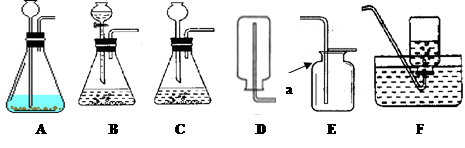
(10海南45)气焊和气割都需要用到乙炔。乙炔俗称电石气(化学式为C2H2),是一种无色无味的气体,密度比空气略小,难溶于水。实验室常用块状固体碳化钙与水反应制备乙炔,该反应比二氧化锰催化过氧化氢分解更加剧烈。请回答:
(1)乙炔的物理性质之一是 ;
(2)图中仪器a的名称是 ;
(3)从下图选择实验室制备乙炔所用仪器的最佳组合是 (填序号)。