(4分)实验室利用右图所示装置进行Na2CO3和NaHCO3热稳定性对比实验。请回答:
(1)加热一段时间后,两试管中石灰水的变化是 。
A.均变浑浊
B.试管1澄清,试管2变浑浊
C.试管2澄清,试管1变浑浊
(2)该实验说明二者中热稳定性强的物质是 (填化学式),另一种物质受热分解的化学方程式是 。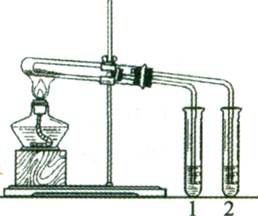
(4分)实验室利用右图所示装置进行Na2CO3和NaHCO3热稳定性对比实验。请回答:
(1)加热一段时间后,两试管中石灰水的变化是 。
A.均变浑浊
B.试管1澄清,试管2变浑浊
C.试管2澄清,试管1变浑浊
(2)该实验说明二者中热稳定性强的物质是 (填化学式),另一种物质受热分解的化学方程式是 。