有机物A可以通过不同化学反应分别制得B、C和D三种物质,结构简式如下图所示。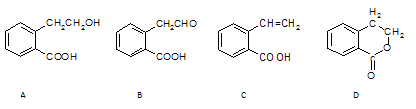
(1)B中的含氧官能团名称是 。
(2) A→C的反应类型是  ;A~D中互为同分异构体的是 。
;A~D中互为同分异构体的是 。
(3)由A生成B的化学方程式是 。
(4)C在一定条件下发生加聚反应的化学方程式是 。
有机物A可以通过不同化学反应分别制得B、C和D三种物质,结构简式如下图所示。
(1)B中的含氧官能团名称是 。
(2) A→C的反应类型是  ;A~D中互为同分异构体的是 。
;A~D中互为同分异构体的是 。
(3)由A生成B的化学方程式是 。
(4)C在一定条件下发生加聚反应的化学方程式是 。