(10分).某有机物结构简式为HOOCCH=CHCHO。
(1)该有机物中各官能团的名称是: ▲ 、 ▲ 、 ▲ 。
(2)检验分子中-CHO的方法是 ▲ ,化学方程式为 ▲ 。
(3)检验分子中 的方法是 ▲ ,化学方程式为 ▲ 。
的方法是 ▲ ,化学方程式为 ▲ 。
(4)实验操作中,-CHO和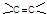 应先检验哪一个
应先检验哪一个 官能团? ▲ 。(填名称)
官能团? ▲ 。(填名称)
(10分).某有机物结构简式为HOOCCH=CHCHO。
(1)该有机物中各官能团的名称是: ▲ 、 ▲ 、 ▲ 。
(2)检验分子中-CHO的方法是 ▲ ,化学方程式为 ▲ 。
(3)检验分子中 的方法是 ▲ ,化学方程式为 ▲ 。
的方法是 ▲ ,化学方程式为 ▲ 。
(4)实验操作中,-CHO和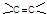 应先检验哪一个
应先检验哪一个 官能团? ▲ 。(填名称)
官能团? ▲ 。(填名称)