(1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需要提供的最低限度的能量叫活化能,其单位通常用kJ·mol-1表示。请认真观察下图,然后回答问题。
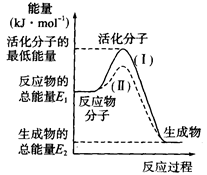
(1)图中所示反应是______(填“吸热”或“放热”)反应,该反应________(填“需要”或“不需要”)加热,该反应的△H=___(用含E1、E2的代数式表示)。
(2)1.00L 1.00 mol·L-1H2SO4溶液与2.00 L 1.00mol·L-1NaOH溶液完全反应,放出114.6kJ热量,表示其中和热的热化学方程式为。
(3)已知16g固体硫完全燃烧时放出148.4kJ的热量,该反应的热化学方程式是。
(4)发射航天器常以联氨(N2H4)为燃料,NO2为推进剂,燃烧生成氮气和水蒸气,火焰温度可达2700℃,已知:N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ/mol ①
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=—534kJ/mol②
对N2H4和NO2反应的说法不正确的是()
| A.N2H4与NO2反应时NO2作氧化剂 |
| B.氮气既是氧化产物,又是还原产物 |
| C.生成1mol N2转移8mol电子 |
| D.该反应的热化学方程式为2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) △H=—1135.7kJ/mol |