(15分)乙酰苯胺具有解热镇痛作用,是较早使用的解热镇痛药,有“退热冰”之称,其制备原理如下:
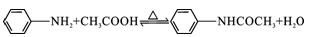
已知:
①苯胺易被氧化。
②乙酰苯胺、苯胺和醋酸的部分物理性质如下表:
物质
|
熔点
|
沸点
|
溶解度
|
乙酰苯胺
|
114.3℃
|
305℃
|
微溶于冷水、易溶于热水
|
苯胺
|
-6℃
|
184.4℃
|
微溶于水
|
醋酸
|
16.6℃
|
118℃
|
易溶于水
|
实验步骤如下:
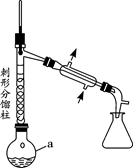
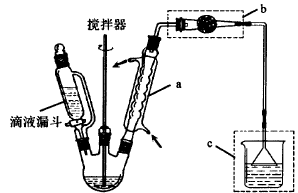
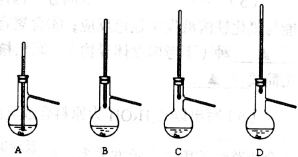
步骤1:在a中,加入9mL (0.10 mol)苯胺、15 mL(0.27 mol)冰醋酸及少许锌粉,依照上图装置组装仪器。
步骤2:控制温度计读数在105℃左右,小火加热回流至反应完全。
步骤3:趁热将反应混合物倒入盛有100 mL 冷水的烧杯中,冷却后抽滤(一种快速过滤方法)、洗涤,得到粗产品。
步骤4:将步骤3所得粗产品进一步提纯后,称得产品质量为10.8g。
请回答下列问题:
(1)仪器a的名称为,所选仪器a的最佳规格是(填序号)。
A.25 mLB.50 mL C.100 mLD.250 mL
(2)实验中加入少许锌粉的目的是。
(3)步骤2中,控制温度计读数在105℃左右的原因是。
(4)判断反应已基本完全的方法为。
(5)步骤3中趁热将混合物倒入盛有冷水的烧杯中,“趁热”的原因是。
(6)步骤4中粗产品进一步提纯,该提纯方法是。
(7)本次实验的产率为。





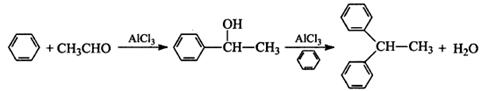

 时认为该离子完全沉淀),应将溶液的pH调至_________(只列算式)以上。
时认为该离子完全沉淀),应将溶液的pH调至_________(只列算式)以上。 粤公网安备 44130202000953号
粤公网安备 44130202000953号