蛇纹石可用于生产氢氧化镁,简要工艺流程如下:
I.制取粗硫酸镁:用酸液浸泡蛇纹石矿粉,过滤;并在常温常压下结晶,制得粗硫酸镁(其中常含有少量Fe3+、Al3+、Fe2+等杂质离子)。
II.提纯粗硫酸镁:将粗硫酸镁在酸性条件下溶解,加入适量的0.1 mol·L-H2O2溶液,再调节溶液pH至7~8,并分离提纯。
III.制取氢氧化镁:向步骤II所得溶液中加入过量氨水。
已知:金属离子氢氧化物沉淀所需pH
|
Fe3+
|
Al3+
|
Fe2+
|
Mg2+
|
开始沉淀时
|
1.5
|
3.3
|
6.5
|
9.4
|
沉淀完全时
|
3.7
|
5.2
|
9.7
|
12.4
|
请回答下列问题:
(1)步骤II中,可用于调节溶液pH至7~8的最佳试剂是(填字母序号)。
A. MgO B. Na2CO3 C. 蒸馏水
(2)Fe2+与H2O2溶液反应的离子方程式为。
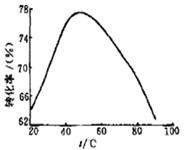
(3)工业上常以Mg2+的转化率为考察指标,确定步骤III制备氢氧化镁工艺过程的适宜条件。其中,反应温度与Mg2+转化率的关系如右图所示。
①步骤III中制备氢氧化镁反应的离子方程式为。
②根据图中所示50 ℃前温度与Mg2+转化率之间的关系,可判断此反应是
(填“吸热”或“放热”)反应。
③图中,温度升高至50 ℃以上Mg2+转化率下降的可能原因是。
④ Ksp表示沉淀溶解平衡的平衡常数。已知:
Mg(OH)2(s)  Mg2+ (aq)+ 2OH- (aq) Ksp = c(Mg2+)·c2(OH-) = 5.6×10-12
Mg2+ (aq)+ 2OH- (aq) Ksp = c(Mg2+)·c2(OH-) = 5.6×10-12
Ca(OH)2(s)  Ca2+ (aq) + 2OH- (aq)Ksp = c(Ca2+)·c2(OH-) = 4.7×10-6
Ca2+ (aq) + 2OH- (aq)Ksp = c(Ca2+)·c2(OH-) = 4.7×10-6
若用石灰乳替代氨水,(填“能”或“不能”)制得氢氧化镁,理由是。