(10分,每空2分)(1)下列反应中属于氧化还原反应的是 。(填序号)
| A.MnO2 + 4HCl(浓)= MnCl2 + Cl2↑+ 2H2O | B.SO2+2H2S = 2H2O+3S↓ |
C.Ba(OH)2 + H2S O4 = BaSO4↓+2H2O O4 = BaSO4↓+2H2O |
D.Cl2+2NaOH =" NaCl" +NaClO+H2O |
(2)已知KMnO 4与浓盐酸发生如下反应:
4与浓盐酸发生如下反应:
2KMnO4 + 16HCl(浓) ="==" 2KCl + 2MnCl2 + 5Cl2↑+8H2O。
在上述反应中,氧化剂是 。用单线桥法标出此反应的电子转移方向和数目。
(3)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:
①将这6种物质分别填入下面对应的横线上,组成一个未配平的化学方程式:
________+________+H2SO4→ ________+________+________(填化学式)
②反应中1mol氧化剂得到______mol电子。
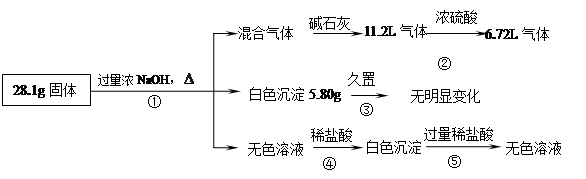
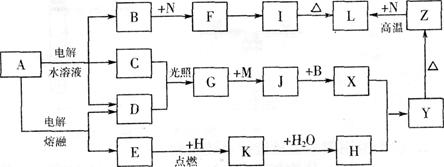
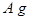 加入FeCl3和盐酸的混合液中,充分反应(不考虑水电离出的离子)。
加入FeCl3和盐酸的混合液中,充分反应(不考虑水电离出的离子)。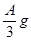 ,则溶液中的阳离子一定有,一定没有;
,则溶液中的阳离子一定有,一定没有;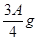 ,则溶液中的阳离子一定有_________,一定没有___________。
,则溶液中的阳离子一定有_________,一定没有___________。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号