(12分)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。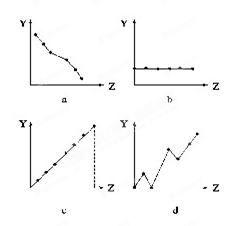
把与下面 元素有关的性质相符的曲线标号填入相应的空格中:
元素有关的性质相符的曲线标号填入相应的空格中:
(1)ⅡA族元素的价电子数____________。
(2)第三周期元素的最高化合价__________。
(3)F-、Na+、Mg2+、Al3+的离子半径________。
(4) 第三周期元素的电负性____________。
(12分)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。
把与下面 元素有关的性质相符的曲线标号填入相应的空格中:
元素有关的性质相符的曲线标号填入相应的空格中:
(1)ⅡA族元素的价电子数____________。
(2)第三周期元素的最高化合价__________。
(3)F-、Na+、Mg2+、Al3+的离子半径________。
(4) 第三周期元素的电负性____________。