(1)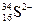 微粒中的质子数是_______,中子数是_______,核外电子数是_______。
微粒中的质子数是_______,中子数是_______,核外电子数是_______。
(2) 1.5mol CO2中含_____ mol碳原子,________个氧原子(以NA为阿伏加德罗常数的值),标准状况下的体积为___________L。
(3)在一定温度和压强下,5体积气体A2跟15体积的气体B2完全化合生成10体积某气体C,则该气体C的化学式为(用A、B表示)__________。
(1)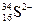 微粒中的质子数是_______,中子数是_______,核外电子数是_______。
微粒中的质子数是_______,中子数是_______,核外电子数是_______。
(2) 1.5mol CO2中含_____ mol碳原子,________个氧原子(以NA为阿伏加德罗常数的值),标准状况下的体积为___________L。
(3)在一定温度和压强下,5体积气体A2跟15体积的气体B2完全化合生成10体积某气体C,则该气体C的化学式为(用A、B表示)__________。