下图中A、B、C、D、E、F、G均为有机化合物。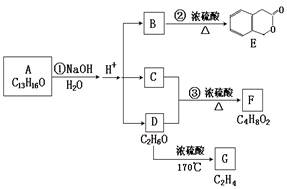
(1)写出反应②的化学反应方程式 。
(2)A的结构简式是 ,反应①的反应类型是
(3)符合下列三个条件的B的同分异构体的数目有 个。
①含有邻二取代苯环结构;②与B具有相同的官能团;
③不可与FeCl3溶液发生显色反应
(4)写出D→G反应方程式
下图中A、B、C、D、E、F、G均为有机化合物。
(1)写出反应②的化学反应方程式 。
(2)A的结构简式是 ,反应①的反应类型是
(3)符合下列三个条件的B的同分异构体的数目有 个。
①含有邻二取代苯环结构;②与B具有相同的官能团;
③不可与FeCl3溶液发生显色反应
(4)写出D→G反应方程式