如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。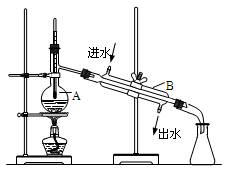
(1)图中有两处明显的错误是
① ;② 。
(2)A仪器的名称是 ,B仪器的名称是 。
(3)实验时A中除加入少量自来水外,还需要加入少量的 ,其作用是 。
如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。
(1)图中有两处明显的错误是
① ;② 。
(2)A仪器的名称是 ,B仪器的名称是 。
(3)实验时A中除加入少量自来水外,还需要加入少量的 ,其作用是 。